《Science》揭秘:女性更易患阿尔茨海默病,四大核心机制颠覆认知
全球约2/3的阿尔茨海默病(AD)患者为女性,这一数据曾被简单归因于女性寿命更长。但《Science》系列顶刊的最新研究彻底颠覆了这一认知,证实女性更高的患病风险,源于雌激素波动、tau病理敏感性、X染色体炎症、APOE基因毒性四大独特生物学机制,并非单纯的寿命差异所致。
PART.01 《科学》新发现:女性AD高风险的四大核心逻辑
1. 雌激素“断崖”:神经保护屏障的突然消失
《Science Advances》2025年研究明确,雌激素是大脑天然的“神经保护剂”,能抑制β淀粉样蛋白(Aβ)沉积、阻断tau蛋白过度磷酸化。女性进入围绝经期后,雌激素水平急剧下降,大脑失去关键保护,Aβ向tau缠结的病理转化进程显著加速。
更关键的是,激素替代治疗存在严格“时间窗”:围绝经期早期干预可降低风险,70岁后使用反而会加快tau沉积与认知衰退,时机直接决定治疗效果。
2. 病理高敏感:女性对Aβ-tau通路的“低耐受”
2026年《JAMA Neurology》研究与《Science》结论高度一致:在相同Aβ负荷下,女性血浆中p-tau217水平显著更高,脑内tau缠结沉积速度更快,认知衰退幅度更大。这一差异独立于年龄与APOE ε4基因,意味着女性大脑对AD核心病理的“耐受度”更低,相同病理损伤下,女性出现症状更早、进展更快。
3. X染色体基因:驱动“双倍炎症”的隐形推手
《Science Translational Medicine》2025年研究揭示,女性拥有两条X染色体,KDM6A基因易发生“逃逸沉默”,导致小胶质细胞过度激活,大脑慢性炎症水平远高于男性。持续的神经炎症是AD进展的核心助推力,会加速神经元死亡,让女性大脑对Aβ、tau的损伤更敏感、更易受损。研究还发现,女性AD患者大脑中S—亚硝基化C3(SNO-C3)的水平高出男性6倍以上,进一步加剧神经损伤,而雌激素下降会促进这种炎症蛋白的产生。
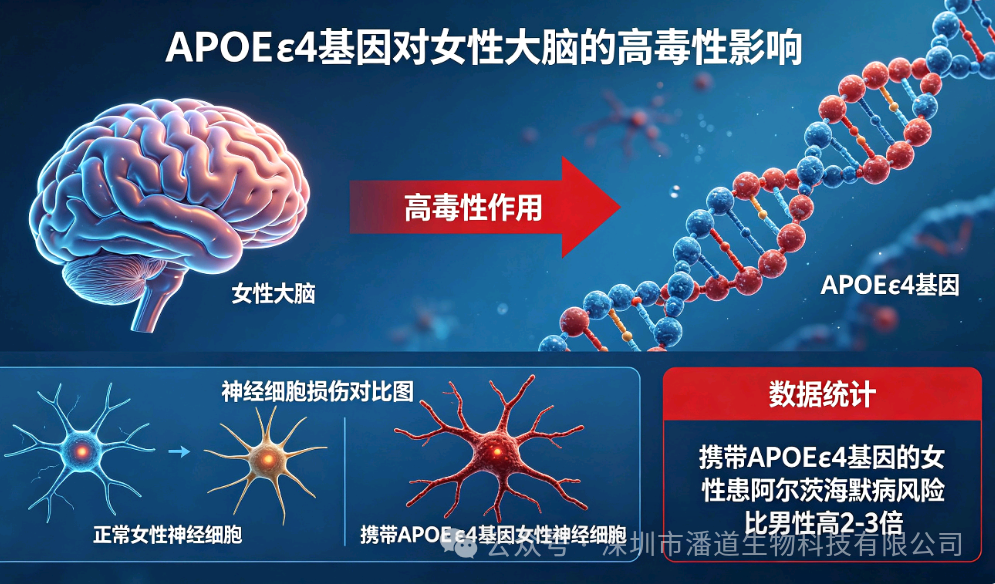
4. APOE ε4:对女性的“毒性”被进一步放大
APOE ε4是目前已知最强的AD风险基因。《Science》综述数据显示,女性携带一个ε4等位基因,患病风险远高于男性携带者。绝经前雌激素可部分缓冲其毒性,绝经后缓冲消失,女性的AD风险被急剧放大,这也是老年女性AD发病率显著攀升的核心原因之一。首都医科大学宣武医院卢洁教授团队研究也证实,女性携带一个APOE ε4等位基因即可导致脑内tau蛋白聚集增加,而男性需携带两个等位基因才会出现明显聚集,进一步佐证了该基因对女性的毒性差异。
PART.02 早筛破局:用精准检测锁定女性AD风险
AD病程隐匿,病理改变在症状出现前10-15年就已启动,传统诊断常陷入“初诊即晚期”的困境。对女性而言,由于病理进展更快、风险更高,早发现、早干预是降低患病风险、延缓病程的唯一有效途径。
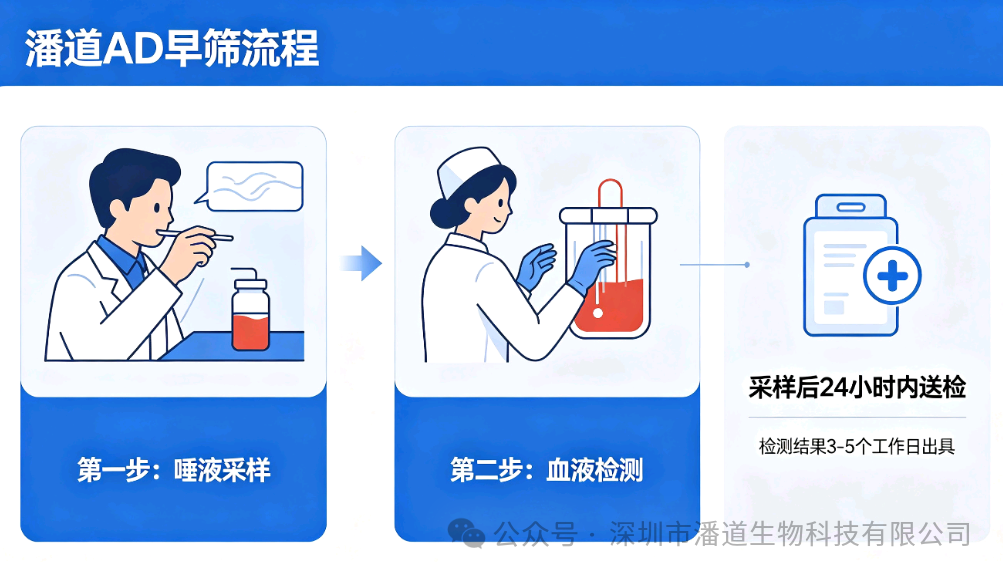
潘道生物聚焦女性AD高风险特征,打造全维度AD早筛体系,覆盖从基因溯源到病理预警的全流程检测,精准匹配当前研究揭示的风险机制:
PART.03 延伸守护:覆盖全生命周期的健康管理
除AD早筛外,潘道生物还针对女性及家庭的健康需求,布局了全场景精准检测项目,构建“AD防控+全维健康”的管理体系:
-
肿瘤与慢病防控:DR-70泛肿瘤早筛检测,可提前5-10年预警多种癌症风险;H型高血压基因检测,精准识别高血压易感基因,指导个性化用药与生活方式干预;高尿酸血症与痛风基因检测,结合血尿酸监测+食疗方案,实现痛风精准管理。
-
过敏与代谢健康:急性过敏原检测,快速锁定过敏诱因,避免反复刺激;酒精检测、抗压能力检测,评估身体代谢与心理应激耐受度,指导科学饮酒与情绪管理。
-
全维基因与细胞健康:医学级人体全套基因检测,覆盖肿瘤、慢病、营养代谢等全维度风险;宠物健康检测,涵盖传染性病原体筛查、遗传基因检测与品种鉴定,守护家人与宠物的共同健康。
女性更易患阿尔茨海默病,是生理结构、激素变化与基因特征共同作用的必然结果。《Science》系列研究的突破,让我们对女性AD风险有了更清晰的认知,也为精准防控指明了方向——早筛、早识别、早干预是守护女性认知健康的关键。
面对持续更新的医学研究与健康需求,潘道生物始终紧跟前沿进展,以临床需求为导向,打造AD早筛+全维健康管理体系。从阿尔茨海默病的基因与病理预警,到肿瘤、慢病、过敏等全场景检测,为女性及家庭提供从预防到干预的全流程健康守护,让每一位女性都能通过精准检测掌握自身健康主动权,从容应对衰老挑战,留住清晰记忆,享受高质量的健康生活。
免责声明
本文仅为医学科学普及知识,并非治疗方案推荐。如需获得治疗方案指导,请咨询专业医师。我们尊重原创,也注重分享,部分图文素材来源于网络,如有违规或侵权,请及时联系,我们将立即做出删除处理。